Die ISO 9001 ist eine Norm, die ähnliche Anforderungen an Qualitätsmanagementsysteme stellt wie die ISO 13485. Obwohl die ISO 9001 nicht für die EU-Medizinprodukteverordnungen (MDR, IVDR) harmonisiert ist, kann sie dennoch in bestimmten Fällen hilfreich oder sogar notwendig sein.
1. Das Zusammenspiel von ISO 9001 und ISO 13485
a) Gemeinsame Historie
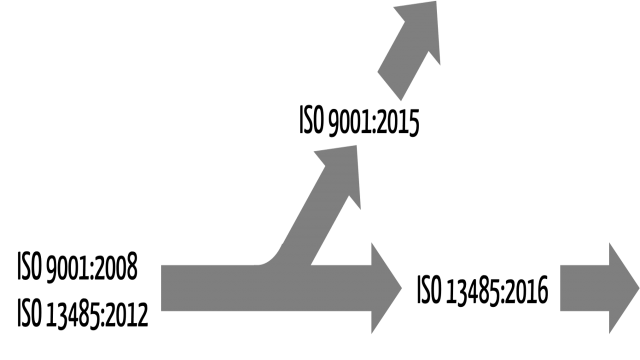
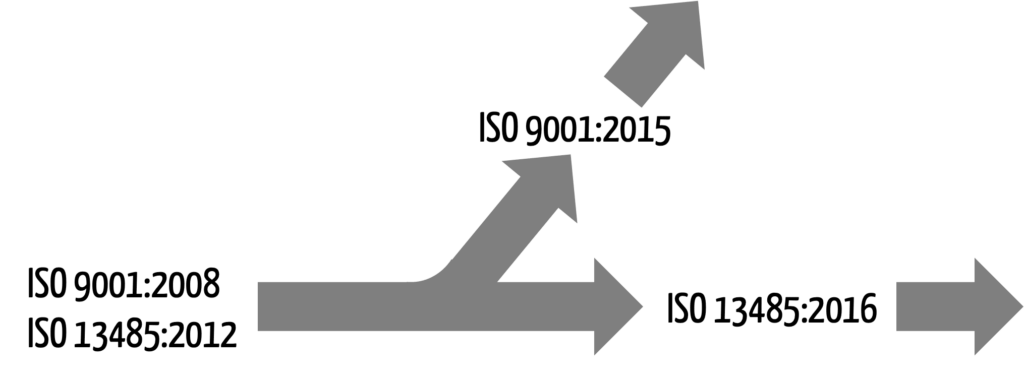
Ursprünglich waren beide Qualitätsnormen fast identisch. Sogar die Kapitelstruktur war völlig gleich. Doch im September 2015 wurde die ISO 9001:2015 in einer grundlegend überarbeiteten Version veröffentlicht, die sich deutlich von der neuesten Version der ISO 13485 unterscheidet. Das Erschweren einer gemeinsamen Zertifizierung nach beiden Normen ist die Folge.
b) Unterschiedliche Zielsetzungen
Die ISO 9001:2015 ist eine “echte Qualitätsmanagementnorm” und legt den Fokus auf die Kundenzufriedenheit. Die ISO 13485 teilt dieses Ziel, aber ihre eigentliche Zielsetzung ist es, die regulatorische Konformität der Hersteller und die Sicherheit der Medizinprodukte zu gewährleisten.
2. Anforderungen der ISO 9001
a) Übersicht
Die ISO 9001 hat immer noch viele gemeinsame Anforderungen mit der ISO 13485, wie beispielsweise die Verpflichtung der Leitung, die Planung eines QM-Systems, die Sicherstellung der notwendigen Ressourcen und die Kontinuierliche Verbesserung.
b) Nennenswerte Unterschiede zwischen den beiden QM-Normen
Der offensichtlichste Unterschied zwischen den beiden Normen besteht darin, dass die ISO 9001 “branchenneutral” ist, während die ISO 13485 ausschließlich auf Medizinprodukte abzielt. Seit der Version 2015 der ISO 9001 sind die Unterschiede jedoch größer geworden. Die ISO 9001 hat eine andere Kapitelstruktur, fordert kein QM-Handbuch und legt mehr Wert auf unternehmensweite Risikobewertungen und Qualitätsziele. Außerdem werden die Anforderungen an die Kommunikation mit Kunden und Lieferanten genauer beschrieben und die Führungsebene noch stärker in die Pflicht genommen.
3. Die Relevanz der ISO 9001 im Kontext von Medizinprodukten
Für die MDR und die IVDR ist nur die ISO 13485 harmonisiert. Daher ist die ISO 9001 wenig hilfreich, um den Nachweis zu erbringen, dass die Anforderungen an ein QM-System erfüllt sind, wie sie in den entsprechenden Artikeln 10 und Anhang IX der MDR und IVDR formuliert sind. Dennoch kann eine Zertifizierung nach ISO 9001 in bestimmten Fällen sinnvoll sein:
- Unternehmen, die nicht nur im Medizinproduktebereich tätig sind und ihr Qualitätsbewusstsein zum Ausdruck bringen möchten.
- Unternehmen, deren Tätigkeiten zwar im Kontext von Medizinprodukten stattfinden, aber nicht ausschließlich in den Anwendungsbereich der ISO 13485 fallen (z.B. Beratungsunternehmen) oder für die die Benannten Stellen nicht akkreditiert sind.
- Unternehmen, die nicht nur die Konformität ihrer eigenen Produkte, sondern auch Anforderungen an das Unternehmensrisikomanagement erfüllen wollen.
- Unternehmen, die die ISO 13485-Zertifizierung aus finanziellen und organisatorischen Gründen nicht benötigen.
Fazit und Zusammenfassung
Die ISO 9001:2015 stellt im Vergleich zur Vorgängerversion eine echte Verbesserung dar. Allerdings ist es bedauerlich, dass die ISO 13485 seit der Version 2016 nicht diesem Beispiel gefolgt ist. Die Anforderungen der ISO 13485 sind anspruchsvoller und insbesondere die Auditoren der Benannten Stellen sind strenger geschult und legen einen größeren Fokus auf diese Norm. Betriebe, die nur nach ISO 9001:2015 zertifiziert sind, haben es daher schwerer, auch ein ISO-13485-Audit zu bestehen.
Änderungshistorie:
- 2023-04-17: Artikel komplett überarbeitet
- 2016-11-08: Erste Version erstellt